Version in American English 🇺🇸 | Versão em Português do Brasil 🇧🇷
🇧🇷 Ozempic e Mounjaro em 2025: dos consultórios às manchetes, a nova era dos remédios para emagrecer
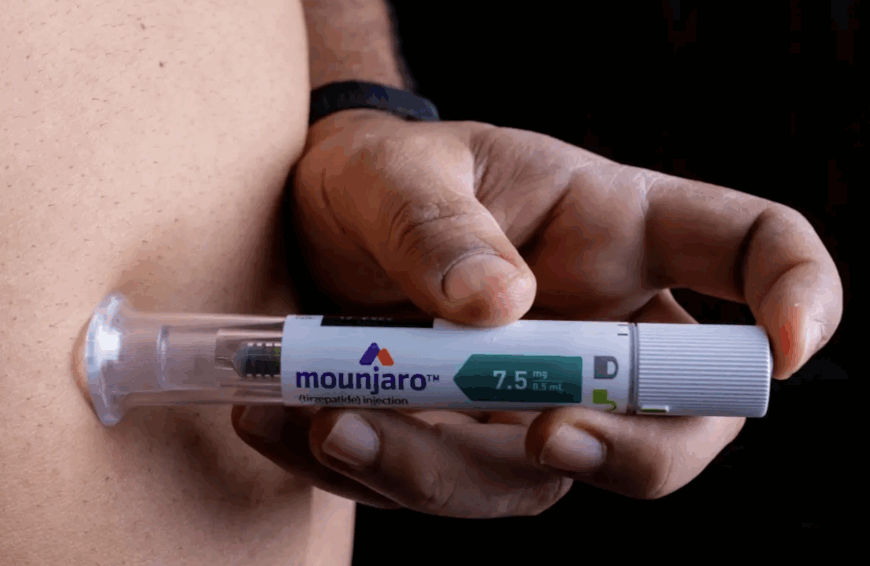
Em poucos anos, dois nomes saltaram do vocabulário técnico da endocrinologia para as conversas de família, rodas de amigos e manchetes de portais de notícia: Ozempic®, à base de semaglutida, e Mounjaro™, que contém tirzepatida. Em 2025, esses medicamentos simbolizam uma mudança de fase no tratamento da obesidade e do diabetes tipo 2 – e também uma mudança na forma como a sociedade enxerga o próprio peso.
O movimento começou nos estudos clínicos, avançou para as diretrizes médicas e, em seguida, ganhou o mundo real. Em consultórios, há histórias de pacientes que, após anos de tentativas frustradas, finalmente viram números consistentes na balança e melhora em exames laboratoriais. Fora deles, houve corrida por receitas, escassez em alguns mercados e debates acalorados sobre uso estético, equidade de acesso e riscos do “remédio da moda”.
Por trás do hype, porém, há um ponto que já não é contestado: os medicamentos funcionam. A discussão em 2025 é outra – como usá-los de forma segura e responsável.
Os efeitos que aparecem primeiro
Na prática clínica, o roteiro é conhecido. Ao iniciar Ozempic ou Mounjaro, muitos pacientes relatam o mesmo conjunto de sensações nas primeiras semanas: náusea, uma sensação de estômago “cheio” com pouca comida, episódios de refluxo, azia e, em alguns casos, perda de interesse pela comida que antes ocupava boa parte do dia.
A lista continua com constipação em boa parte dos usuários e, na outra ponta, diarreia em alguns casos. Tontura leve, cansaço e uma espécie de “descompasso” com a própria fome também entram no pacote de adaptação.
Não se trata de surpresa: esses medicamentos retardam o esvaziamento gástrico, modulam a liberação de hormônios relacionados à saciedade e alteram a forma como o corpo lida com glicose. O organismo responde, e essa resposta tem rosto, horário e incômodo.
Como os médicos têm contornado os efeitos colaterais
Se nas redes sociais o assunto costuma aparecer em tom de polêmica, nas consultas o clima é mais pragmático. Médicos já sabem que a forma de iniciar o tratamento pesa tanto quanto a dose final.
Em 2025, tornou-se quase um consenso entre especialistas:
- escalonar a dose devagar, respeitando o tempo de adaptação de cada paciente, reduz o risco de náusea intensa e vômitos;
- fracionar as refeições e comer devagar diminui sensações de peso e refluxo;
- hidratar-se ao longo do dia, em vez de ingerir grandes volumes de líquido de uma só vez, alivia tontura e ajuda o intestino a funcionar;
- priorizar proteínas e fibras e evitar, sobretudo no início, refeições muito gordurosas e álcool reduz significativamente os desconfortos digestivos.
Com essas medidas simples, uma parte importante dos efeitos colaterais deixa de ser motivo para abandono do tratamento.
Os riscos que exigem vigilância
Os eventos mais graves ligados a essa classe de medicamentos continuam sendo raros, mas estão no radar. Casos de pancreatite despertam atenção sempre que há dor abdominal intensa e persistente. Problemas na vesícula, como formação de cálculos, aparecem com mais frequência em quadros de perda de peso rápida – algo comum entre usuários de Ozempic e Mounjaro.
Em pacientes com diabetes tipo 2 que já utilizam outros antidiabéticos, o risco de hipoglicemia exige ajustes finos de dose e monitorização mais próxima. Fora desse grupo, o problema é menos frequente, mas não desprezível.
Semaglutida x tirzepatida: diferenças na prática
Na comparação do mundo real, a tirzepatida tem se destacado por proporcionar perdas de peso um pouco mais expressivas que a semaglutida. O perfil de efeitos colaterais, porém, é bastante parecido: náuseas e alterações gastrointestinais dominam o início do tratamento em ambos os casos.
A escolha entre um e outro, em 2025, tende a levar em conta o histórico clínico, o grau de obesidade, a presença de diabetes, a resposta prévia a outras medicações e, não menos importante, custo e disponibilidade.
Além da balança: o debate que não termina na consulta
Enquanto a ciência avalia impacto cardiovascular, desfechos a longo prazo e segurança em grupos específicos, a sociedade discute outro lado da história. A popularização de Ozempic e Mounjaro reacende questões sobre:
- medicalização da estética,
- prioridades de acesso entre pacientes com indicação clínica e uso meramente cosmético,
- impacto psicológico de depender de uma injeção semanal para controlar o peso.
No meio desse cruzamento de interesses, um ponto desponta como eixo comum: informação qualificada. Em 2025, a grande diferença não está apenas na existência desses medicamentos, mas na forma como médicos, pacientes e a opinião pública escolhem lidar com eles – com euforia ou com equilíbrio.
Em um cenário em que a obesidade é reconhecida como doença crônica e complexa, Ozempic e Mounjaro não encerram o problema, mas mudam o tabuleiro. O desafio, daqui em diante, é usá-los com a mesma inteligência com que foram desenvolvidos.
🇺🇸 Ozempic and Mounjaro in 2025: from clinic routine to global spotlight
In just a few years, two drug names have moved from specialist vocabulary to casual conversation: Ozempic®, based on semaglutide, and Mounjaro™, which contains tirzepatide. By 2025, they have come to represent a turning point in the treatment of obesity and type 2 diabetes – and, in many ways, a shift in how society discusses weight.
The story began in clinical trials, moved into medical guidelines, and quickly spilled into real life. Doctors now describe patients who, after countless unsuccessful attempts, finally experienced consistent weight loss and improvements in lab results. Outside the clinical setting, shortages, celebrity mentions, black-market offers and heated debates emerged – about aesthetic use, fairness in access, and the risks of turning a prescription drug into a wellness trend.
But beneath the noise, one point is no longer controversial: these medications work.
The conversation in 2025 is less about whether they are effective, and more about how to use them responsibly.
The side effects that show up first
In real-world practice, the early phase of treatment follows a familiar script. Once Ozempic or Mounjaro is started, many patients report similar sensations: nausea, an unusual feeling of fullness after very small meals, episodes of heartburn or reflux, and – for some – a near-complete loss of appetite.
Constipation is extremely common; when ignored, it can linger for months. Others experience the opposite – brief episodes of diarrhea. Lightheadedness and fatigue may occur when eating habits shift too suddenly or when hydration falls behind.
None of this surprises clinicians. These medications slow gastric emptying, alter appetite-regulating hormones, and change the body’s relationship with glucose. The gut reacts – and that reaction often determines whether the patient continues treatment.
How physicians are navigating these downsides
Far from the dramatic tone of social media, the clinical approach is more methodical. Physicians have learned that the way treatment begins matters as much as the medication itself.
By 2025, several strategies have become standard in clinics around the world:
- increasing the dose gradually, in a pace that respects individual tolerance;
- encouraging smaller, slower meals to ease digestive discomfort;
- spreading fluid intake throughout the day, rather than in large volumes at once;
- ensuring adequate protein and fiber to protect lean mass during weight loss;
- limiting high-fat meals and alcohol, especially in the first weeks, when nausea is more likely.
When these measures are followed, many of the symptoms that once led patients to quit early become manageable.
The uncommon – but important – risks
Serious complications remain rare, but well-documented. Cases of pancreatitis draw immediate attention when persistent upper abdominal pain appears. Gallstones are more likely in individuals experiencing rapid weight loss – a common outcome among strong responders.
In patients with type 2 diabetes who are already taking other glucose-lowering medications, the risk of hypoglycemia requires careful adjustments. Outside this group, low blood sugar is uncommon but still monitored.
Semaglutide vs. tirzepatide: what real-world data suggest
Everyday clinical experience points to a consistent trend: tirzepatide often produces greater weight loss than semaglutide. But the general tolerability profile – dominated by gastrointestinal symptoms – remains similar between the two.
Choosing between them in 2025 usually depends on clinical history, presence or absence of diabetes, previous treatment attempts, patient preference, and, in many places, cost and availability.
Beyond the scale: the broader debate
While researchers continue to study long-term safety and cardiovascular outcomes, the public discussion has widened. The popularity of these drugs forces society to confront questions about:
- the line between medical treatment and aesthetic pressure;
- how to prioritize access when supply is limited;
- the psychological impact of relying on a weekly injection to manage weight.
Somewhere between hype and skepticism, one point has become central: the quality of information. What distinguishes 2025 from the early rush is not just scientific data – but the maturity with which doctors, patients, and journalists have learned to approach the subject.
In a world where obesity is increasingly recognized as a chronic, multifactorial disease, Ozempic and Mounjaro do not close the chapter. They open a new one. The next steps depend on how responsibly these tools are used – and how well society understands their role.